O que é amônia? Fórmula e propriedades da amônia
A amônia é um composto que é o mais importanteuma fonte de nitrogênio para organismos vivos, e também encontrou uso em várias indústrias. O que é amônia, quais são suas propriedades? Vamos descobrir.
O que é amônia: as principais características
A amônia (nitreto de conduto de água) é um composto de nitrogênio com hidrogênio, tendo a fórmula química NH3. A forma da molécula se assemelha a uma pirâmide trigonal com o átomo de nitrogênio em seu ápice.

A amônia é um gás que não tem cor, mas tem um cheiro forte e específico. A densidade da amônia é quase metade da do ar. A uma temperatura de 15 oC é 0,73 kg / m3. A densidade do líquido de amônia em condições normais é de 686 kg / m3. O peso molecular da substância é de 17,2 g / mol. Uma característica distintiva da amônia é sua alta solubilidade em água. Assim, a uma temperatura de 0 ° C, o seu valor atinge cerca de 1200 volumes no volume de água, a 20 ° C - 700 volumes. A solução "amônia-água" (água de amônia) é caracterizada por uma reação ligeiramente alcalina e uma propriedade bastante única em comparação com outros álcalis: com concentração crescente, a densidade diminui.
Como se forma a amônia?
O que é amônia no corpo humano? Este é o produto final do metabolismo de nitrogênio. A maior parte do fígado se converte em uréia (carbamida) - uma substância menos tóxica.
A amônia em condições naturais é formada como resultado da decomposição de compostos orgânicos contendo nitrogênio. Para uso na indústria, esta substância é produzida por meios artificiais.
Produção de amônia em condições industriais e laboratoriais
Em condições industriais, a amônia é produzida por síntese catalítica de nitrogênio e hidrogênio:
N2 + 3H2 → 2NH3 + Q.
O processo de obtenção da substância é realizado emtemperatura de 500 ° C e uma pressão de 350 atm. O ferro poroso é usado como catalisador. A amônia resultante é removida por resfriamento. O nitrogênio e o hidrogênio, que não reagiram, retornam à síntese.
Em condições de laboratório, a amônia é produzida principalmente pelo aquecimento moderado de uma mistura que consiste em cloreto de amônio e cal hidratada:
2NH4Cl + Ca (OH)2 → CaCl2 + 2NH3↑ + 2H2O.
Para secagem, o composto acabado é passado através de uma mistura de cal e soda cáustica. Amônia bem seca pode ser obtida dissolvendo-se sódio metálico e depois destilando.
Onde a amônia é usada?
Nitreto de hidrogênio é amplamente utilizado em váriosindústrias. Enormes quantidades são utilizadas para a produção de ácido nítrico e vários fertilizantes (uréia, nitrato de amônio, etc.), polímeros, ácido cianídrico, soda, sais de amônio e outros produtos químicos.

Na indústria leve, as propriedades da amôniaEles são usados para limpeza e pintura de tecidos como seda, lã e algodão. Na produção de aço, é usado para aumentar a dureza do aço, saturando suas camadas superficiais com nitrogênio. Os resíduos ácidos são neutralizados na indústria petroquímica com a ajuda do nitreto de hidrogênio.
Devido às suas propriedades termodinâmicas, a amônia líquida é usada como refrigerante em equipamentos de refrigeração.
Uma solução de nitreto de hidrogênio (amônia) é usada na medicina para remover do desmaio, estimulação do vômito, para lidar com as mãos do corpo clínico, com picadas de insetos, etc.

Algumas propriedades químicas da amônia
O nitreto de hidrogênio é caracterizado por uma atividade química bastante alta e é capaz de reagir com muitas substâncias.
Quando a amônia reage com ácidos, os sais de amônio correspondentes são formados. Assim, por exemplo, como resultado da reação com o ácido nítrico, forma-se o nitrato de amônio:
NH3 + HNO3 → NH4NÃO3.
Na reação com o HCl, o cloreto de amônio é formado:
NH3+ HCl → NH4Cl.

Os sais de amônio são sólidossubstâncias cristalinas, decompondo-se em água e possuindo as propriedades inerentes aos sais metálicos. Soluções de compostos formados como resultado da interação de amônia e ácidos fortes têm uma reação fracamente ácida.
Devido aos átomos de nitrogênio, o nitreto de hidrogênio éagente redutor ativo. Suas propriedades redutoras são manifestadas quando aquecidas. Quando queima em uma atmosfera de oxigênio, forma nitrogênio e água. Na presença de catalisadores, a interação com o oxigênio dá óxido nítrico. O nitreto de hidrogênio tem a capacidade de reduzir metais de óxidos.
Os halogênios formam uma reação com amôniaHaletos de nitrogênio são explosivos perigosos. Ao interagir com os ácidos carboxílicos e seus derivados, o nitreto de hidrogênio forma amidas. Em reações com carvão (a 1000 ° C) e metano, dá ácido cianídrico.
Com íons metálicos, a amônia forma aminocomplexos,ou amônia (compostos complexos) com uma característica: um átomo de nitrogênio está sempre ligado a três átomos de hidrogênio. Como resultado da complexação, a cor da substância muda. Assim, por exemplo, uma solução azul de sulfato de cobre com a adição de nitreto de hidrogênio adquire uma cor azul-violeta intensa. Muitos dos aminocomplexos possuem estabilidade suficiente. Devido a isso, eles podem ser obtidos em forma sólida.

Na amônia líquida, os compostos inorgânicos e orgânicos iônicos e não polares são facilmente solúveis.
Características sanitárias e higiênicas
A amônia é classificada como a quarta classe de risco. A concentração máxima máxima permitida (MPC) no ar dos assentamentos é de 0,2 mg / m3, a média diária - 0,04. No ar da área de trabalho, o teor de amônia não deve estar acima de 20 mg / m³. Em tais concentrações, o cheiro da substância não é sentido. É fixado com olfato humano a 37 mg / m³. Ou seja, se o cheiro de amônia é sentido, isso significa que os padrões permissíveis para a presença de matéria no ar são significativamente excedidos.
Influência no corpo humano
O que é amônia em termos de impacto sobrea pessoa? É um tóxico. É classificado como uma substância capaz de exercer um efeito sufocante e neurotrópico, envenenamento por inalação que pode levar a edema pulmonar e danos ao sistema nervoso.
O vapor de amônia irrita a peletampas, membranas mucosas dos olhos e órgãos respiratórios. A concentração da substância na qual a faringe está irritada é de 280 mg por metro cúbico. metro, olho - 490 mg por metro cúbico. metro. Dependendo da quantidade de nitreto de hidrogênio no ar, pode haver um inchaço na garganta, dificuldade para respirar, ataques de tosse, dor ocular, lacrimejamento profuso, queimadura química da córnea, perda de visão. Com um teor de amônia de 1,5 g por metro cúbico. metro por uma hora desenvolve edema pulmonar tóxico. Quando a amônia líquida e suas soluções (em altas concentrações) entram em contato com a pele, vermelhidão, coceira, ardor, dermatite são possíveis. Como o nitreto liquefeito do conduto de água absorve o calor durante a evaporação, é possível a congelação de vários graus.
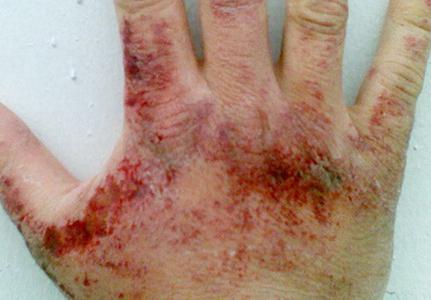
Sintomas de envenenamento com amônia
O envenenamento por este agente tóxico pode causaruma diminuição no limiar auditivo, náusea, tontura, dor de cabeça, etc. Pode haver mudanças no comportamento, em particular uma forte excitação, delírio. A manifestação de sintomas em vários casos é intermitente. Eles podem cessar por um tempo e depois renovar com vigor renovado.
Levando em conta todas as possíveis conseqüências da exposição à amônia, é muito importante observar precauções ao trabalhar com esta substância e não exceder sua concentração no ar.
</ p>


